Раствор представляет собой гомогенную смесь, состоящую из двух или более веществ, а растворимость - это максимальное количество соединения или вещества, которое может растворяться в ряде растворителей .
Многие решения, с которыми мы сталкиваемся в повседневной жизни, включают стакан сладкого сиропа. В стакане сиропа несколько компонентов: вода, сироп и сахар.
Если эти компоненты смешать вместе до тех пор, пока составляющие компоненты больше не будут видны, то получится раствор.
Обсуждая решение, следующий дальнейший обзор включает определение, свойства, типы и факторы решения.
Определение раствора и растворимости

Решение
Раствор - это однородная смесь, состоящая из двух и более веществ. Вызывается решением из-за компонентов раствора.
В растворе есть растворители и растворенные вещества. Растворенное вещество (растворенное вещество) - это вещество, которое составляет раствор, количество которого в растворе меньше. Между тем, растворитель (растворитель) - это вещество, которого больше, чем растворенного вещества.
Состав морского вещества в растворе выражается концентрацией раствора. В то время как процесс смешивания растворенного вещества и растворителя с образованием раствора называется растворением или сольватацией.
Чтобы понять больше о решении, рассмотрите следующую иллюстрацию.
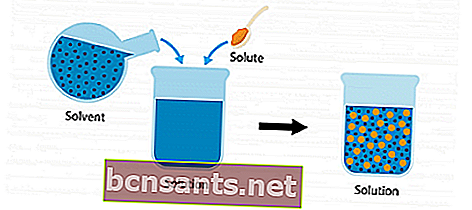
Есть растворенное вещество и растворитель. Когда два ингредиента смешиваются и объединяются в контейнере, получается раствор.
Растворимость (и)
Под растворимостью понимается максимальное количество соединения или вещества, которое может растворяться в ряде растворителей.
Растворимость обозначается буквой s (растворимость) в единицах моль / л или обычно используется единицы молярности M. Вот формула растворимости или молярности.
M = n / V
где M - молярность (моль / л), n - количество молей вещества (моль), V - объем раствора или растворителя (л).
Растворимость также определяется как концентрация вещества, которое все еще может растворяться в определенном количестве растворителя.
Произведение постоянной растворимости (Ksp)
Растворенное вещество, растворенное в растворителе, образует равновесную реакцию. На возникновение равновесия влияют нерастворимые растворенные вещества и растворенные ионы.
Также прочтите: 100+ примеров стандартных и нестандартных слов + пояснения [ОБНОВЛЕНО]Ниже приводится пример константы равновесия для реакции.
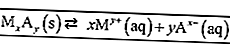
В соответствии с правилами написания формулы равновесия, в формулу записываются только вещества в виде раствора (водного) и газа (ов). Так что получается:
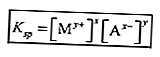
Константа равновесия трудно растворяемого раствора называется константой произведения растворимости (Ksp).
Свойства решения

Физические свойства, которые проявляются в растворе, делятся на три, а именно:
1. Коллигативные свойства решений.
Это характеристика раствора, которая зависит от количества частиц растворенного вещества в растворе и не зависит от типа частиц растворителя.
Коллигативные свойства эквивалентны концентрации различных неэлектролитных веществ в растворе независимо от типа или химических свойств составляющих.
При определении коллигативных свойств раствора твердых веществ в жидкости твердое вещество считается нелетучим, а давление пара над раствором полностью зависит от растворителя.
Некоторые из коллигативных свойств раствора - осмотическое давление, снижение давления пара, повышение температуры кипения и снижение температуры замерзания.
2. Аддитивные свойства
В растворе аддитивные свойства - это свойства раствора, которые зависят от общего количества атомов в молекуле или от числа составляющих свойств раствора.
Примером аддитивных свойств растворов является молекулярная масса, которая является суммой атомных масс.
Масса компонентов раствора включается в свойства добавки, общая масса раствора - это количество каждого компонента раствора, а именно растворенного вещества и растворителя.
3. Конституционный характер
Это включает в себя природу раствора, которая зависит от атомов в молекуле (от типа атома и количества атомов). Его конститутивные свойства указывают на правила отдельных соединений и групп молекул в системе.
Есть несколько физических свойств, которые частично являются аддитивными и определяющими. К ним относятся преломление света, электрические свойства, поверхностные и межповерхностные свойства, которые включены в некоторые составляющие и некоторые добавки.
Тип решения

1. Ненасыщенный раствор
Ненасыщенный раствор означает раствор, который содержит меньше растворенных веществ, чем необходимо для получения насыщенного раствора. Ненасыщенные растворы содержат частицы, которые не прореагировали должным образом с веществом, другими словами, они все еще могут растворять вещество.
Раствор считается ненасыщенным, если значение концентрации ионов <Ksp. В ненасыщенном растворе не происходит отложения растворенных веществ.
Также прочтите: Определение химических растворов, их типов и компонентов.2. Насыщенный раствор.
Раствор включается в насыщенный раствор, когда существует равновесие между растворенным веществом и растворителем. В насыщенном растворе частицы точно реагируют с реагентом или достигают максимальной концентрации.
Считается, что раствор насыщен, если концентрация ионов равна значению Ksp. В этом состоянии равновесия скорость растворенного вещества в растворителе такая же, как скорость, с которой оно оседает. То есть концентрация вещества в растворе одинакова.
3. Сильнонасыщенный раствор.
Это раствор, который содержит больше растворенного вещества, чем растворитель. Это приводит к тому, что значение продукта концентрации ионов> Ksp, так что раствор насыщается и оседает.
Фактор растворимости

Растворимость жидкости варьируется. На это влияет несколько факторов растворимости. Вот некоторые из факторов растворимости.
1. Температура
Уровень температуры раствора влияет на процесс растворения растворенного вещества. При более высоких температурах растворенное вещество легко растворяется в растворителе.
Это происходит потому, что твердые частицы при более высоких температурах движутся быстрее, что обеспечивает более частые и эффективные столкновения.
2. Размер растворенного вещества.
Чем меньше гранулы растворенного вещества, тем легче он растворяется в растворителе. Небольшое количество гранул растворенного вещества приводит к увеличению площади поверхности вещества и его растеканию в растворе.
Чем больше площадь поверхности вещества, тем больше частиц сталкивается друг с другом. Это то, что заставляет процесс растворения происходить быстрее.
3. Объем растворителя
Большой объем растворителя влияет на процесс растворения вещества. Это связано с тем, что все больше и больше частиц растворителя вступают в реакцию с растворенным веществом.
Чем больше используется растворитель, тем быстрее будет процесс растворения растворенного вещества.
4. Скорость перемешивания
Если вы добавите фактор перемешивания, процесс растворения ускорится.
При перемешивании частицы растворенного вещества все больше смешиваются с растворителем, так что реакция растворения идет быстрее, чем растворение без перемешивания.
Это объяснение решения и растворимости, а также значения, свойств, типов и факторов. Может быть полезно.
